- 当前位置:
- 首页
- >
- 成果转换
- >
- 基于保守的生物学特征开发的肿瘤早期诊断标志物
基于保守的生物学特征开发的肿瘤早期诊断标志物
- 分享到:
 项目计划总投入:200万元
项目计划总投入:200万元 奖励金额:面议
奖励金额:面议  单位名称:厦门大学医学院
单位名称:厦门大学医学院 所属领域:生物医药与大健康
所属领域:生物医药与大健康 技术需求类型:关键难题
技术需求类型:关键难题 期望合作方式:联合开发
期望合作方式:联合开发 联系人:秦**
联系人:秦** 联系电话:15186749026
联系电话:15186749026
我要揭榜

 成果介绍
成果介绍
已发表研究成果
①首次在泛癌组织水平鉴定高度保守的DNA甲基化标签,并运用多组学揭示不同生物学过程的甲基化标签的内外在决定因子(《Genome Medicine》,2024,IF 12.3,第一作者)。申请人在泛肿瘤DNA甲基化水平提取的不同生物学过程驱动的保守性DNA甲基化标签,明确FOXA1-TP53驱动的保守性的甲基化标签Hypo-MS4与肿瘤免疫微环境和免疫应答有关。本次申请的是此研究工作的延续,采用该方法首次在肝癌血液水平提取保守的肿瘤DNA甲基化标签,并解释血液的DNA甲基化标签背后的驱动因素,为肝癌的早期诊断提供新的高度特异性的诊断标志物,同时为肝癌的早期治疗提供新的线索。
主要研究内容如下:
癌症的发生是由组织内外部的因素诱导发生,研究表明外部环境的影响包括,年龄,抽烟,喝酒和紫外线照射等均会诱发肿瘤的发生。内部因素包括基因组的改变,组织内微环境的变化等与肿瘤的发生紧密相关。申请人前期研究基于大规模的泛肿瘤组织(9种肿瘤组织)的表观基因组的DNA甲基化,采用超大矩阵的置换检验及非负矩阵分解法首次在泛肿瘤提取出一系列高度保守的DNA甲基化标签(DNA methylation signature)(图1)。
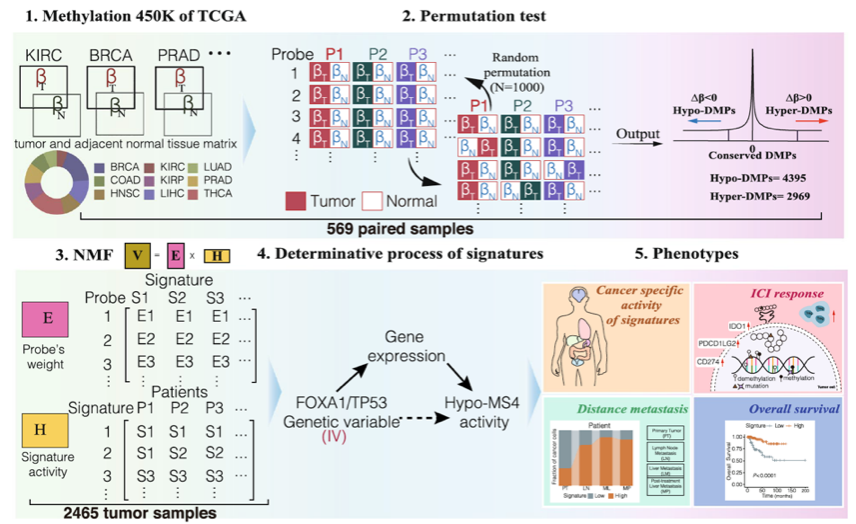
图1 泛肿瘤水平的DNA甲基化标签提取的流程图
申请人对这些保守的DNA甲基化标签的表型分析发现免疫特异性的DNA甲基化标签,在多个肿瘤中,DNA甲基化标签的在结肠癌中的活性与肿瘤的远处转移有关。在黑色素瘤和胃癌中,申请人发现DNA甲基化标签活性与免疫治疗应答紧密相关(图2)。这提示,DNA甲基化活性可作为免疫治疗的伴随诊断的标志物。
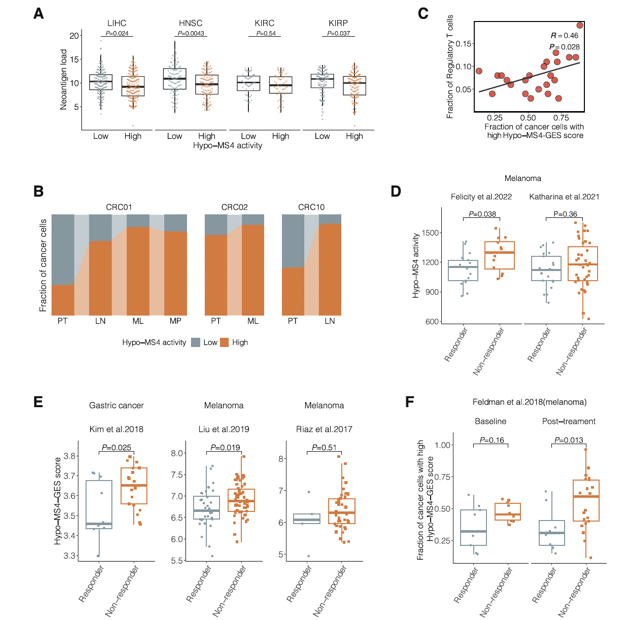
图2 保守的DNA甲基化标签与肿瘤免疫相关
申请人采用工具变量及转录因子的分析,鉴定了每个保守的DNA甲基化标签的驱动因素。包括泛肿瘤的DNA甲基化标签与免疫紧密相关,其驱动基因为FOXA1和TP53(图2),肝癌特异性的DNA甲基化标签的驱动基因为NRF2和KEAP1(图3)。
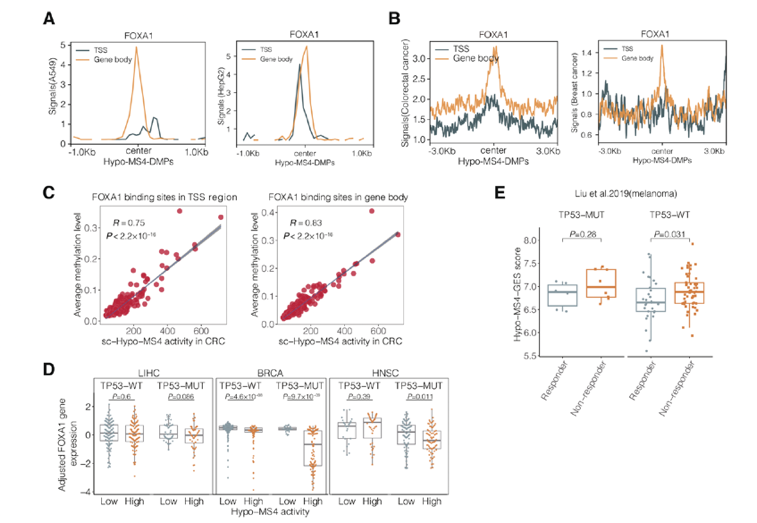
图3 FOXA1的结合和TP53的突变驱动免疫特异性的DNA甲基化标签
申请人评估DNA甲基化标签的活性变化对肿瘤患者临床预后的影响。首先排除治疗对患者免疫作用的影响,在患者未受干预的前提下,肿瘤更高新抗原负荷的患者里(热肿瘤),DNA甲基化标签的活性增高与患者更差的生存显著相关(图4)。这提示,DNA甲基化活性可作为肿瘤患者预后的标志物。
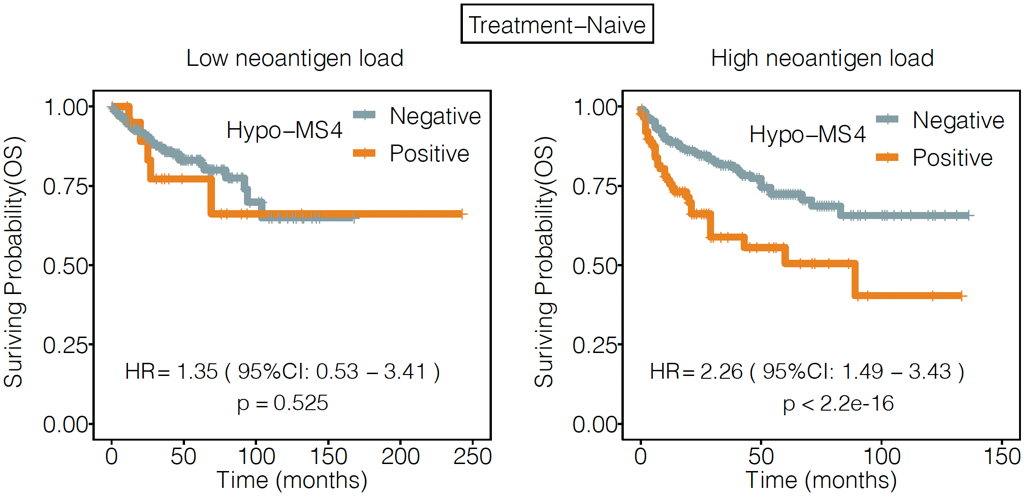
图4 DNA甲基化标签活性的与患者生存的关系
评估DNA甲基化标签的驱动基因FOXA1表达量的变化对肿瘤患者的临床预后的影响作用,研究结果表明,高新抗原负荷(热肿瘤),MKI67高表达(高增值癌细胞)的患者FOXA1的基因表达量降低,患者的预后更差(图5)。这提示对于肿瘤异质性的增强的患者里,FOXA1的表达量可作为患者不良预后的指标,同时也提示免疫相关的DNA甲基化标签的产生。可采用精准治疗的方法(靶向DNA甲基化标签活性)为患者提供新的治疗方案。
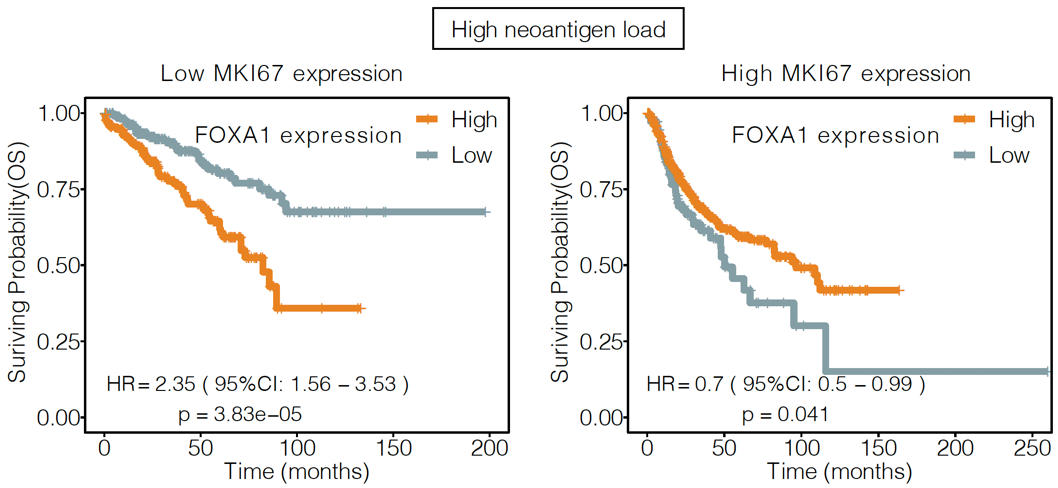
图5 FOXA1基因表达与患者生存的关系
②初步探索在乳腺癌里提取的DNA甲基化标签为乳腺癌的早期诊断提供潜在的诊断标志物,并且该标志物同时能够预测患者的免疫治疗应答(《Frontiers in Genetic》,2024,IF 2.8,通讯作者)。为了进一步探究DNA甲基化水平的异常与肿瘤免疫的相关性,我们在乳腺癌血液中游离的DNA甲基化同样提取到保守性的甲基化标签,并且鉴定保守性的DNA甲基化标签与早期肿瘤的发生有关,并在血液水平鉴定了特定的甲基化位点能够预测肿瘤的发生和患者免疫治疗的应答
主要研究内容如下:
申请人采用早期提取DNA甲基化标签的方法应用于乳腺癌组织,探究组织来源的DNA甲基化标签的是否能作为血液肿瘤源的DNA甲基化的早期诊断标志物,提取到保守的DNA甲基化标签,并且标签的活性与肿瘤的早期发生显著相关(图6)。
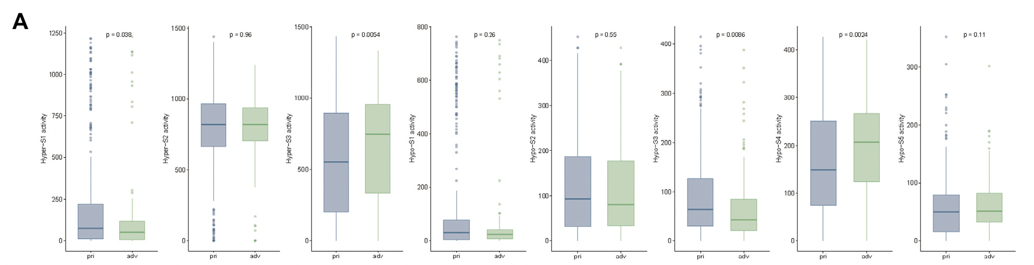
图6 乳腺癌的DNA甲基化标签活性与肿瘤分期的关系
分析与肿瘤分期相关的DNA甲基化的具体的探针(N=510)在血液里的水平与早期肿瘤的发生显著相关(P < 0.05)。进一步分析这510个探针,发现有23个探针同时与肿瘤免疫有关,能够有效预测免疫应答(图7)
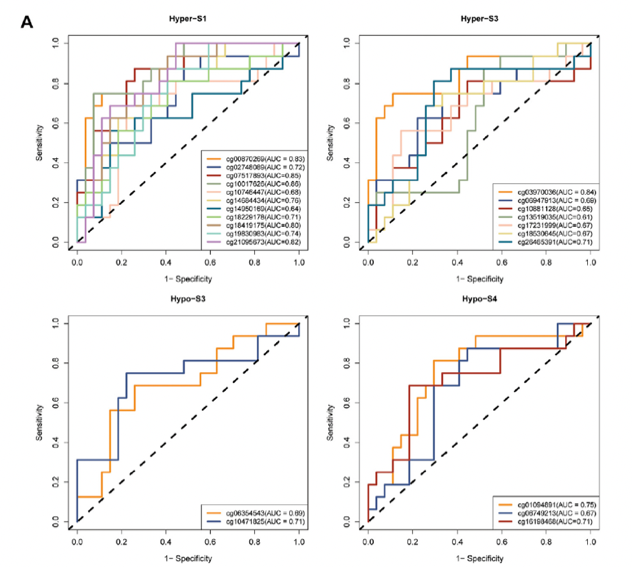
图7 甲基化标签对应探针对肿瘤免疫应答的预测效力
未发表的研究成果
肝癌特异性甲基化标签与肿瘤的早期诊断
1.肝癌的特异性甲基化标签与肿瘤分期的关系
申请人在前期泛癌组织水平提取到肿瘤保守的DNA甲基化标签,揭示保守的DNA甲基化标签的驱动因素和临床表型紧密相关。与缺氧环境有关的甲基化标签是肝癌特异性的(图 8A,P < 2.22)。因此,申请人初期探究缺氧环境有关的DNA甲基化标签与肿瘤早期发生显著相关,包括肿瘤早期和晚期(图8B,P = 0.036),肿瘤病理早期包括的T1和T2期(图8C,P = 0.0047)。以上结果均表明,缺氧有关的DNA甲基化标签具有肿瘤特异性,在肿瘤发生早期阶段其活性显著升高,提示DNA甲基化标签可能成为潜在的肿瘤早期诊断标志物。
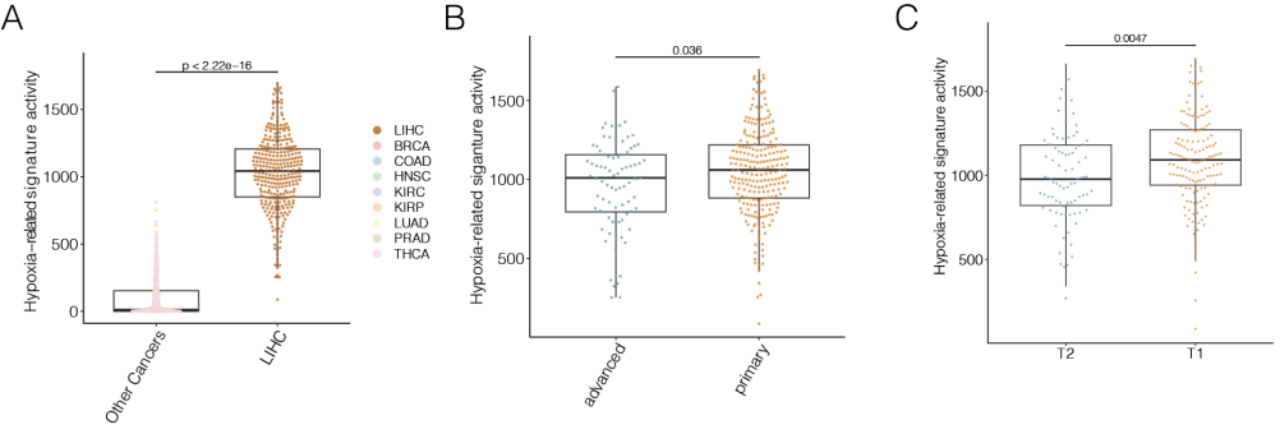
图8 缺氧有关的DNA甲基化标签与肿瘤分期的关系
2.考察肿瘤游离DNA甲基化标签的活性
本申请人收集了22例肝癌和22例肝炎,及20例正常人的血液的DNA甲基化数据,假设血液水平与组织水平的缺氧有关的甲基化标签是一致的,采用组织水平的缺氧有关的甲基化标签的探针在血液里提取对应的甲基化标签,考察其活性在肝癌血液水平是否如组织一样显著升高的。结果显示,血液水平的缺氧有关的DNA甲基化标签的活性显著低于对照组,包括肝癌与肝炎(图9A,),肝癌与正常人(图9B,)。这提示,组织水平缺氧的DNA去甲基化标签的活性降低。但是DNA去甲基化活性降低的背后的驱动因素是未知的。因此,我们需要在血液里单独提取保守的DNA甲基化标签,解释血液水平的DNA甲基化发生的生物学过程。
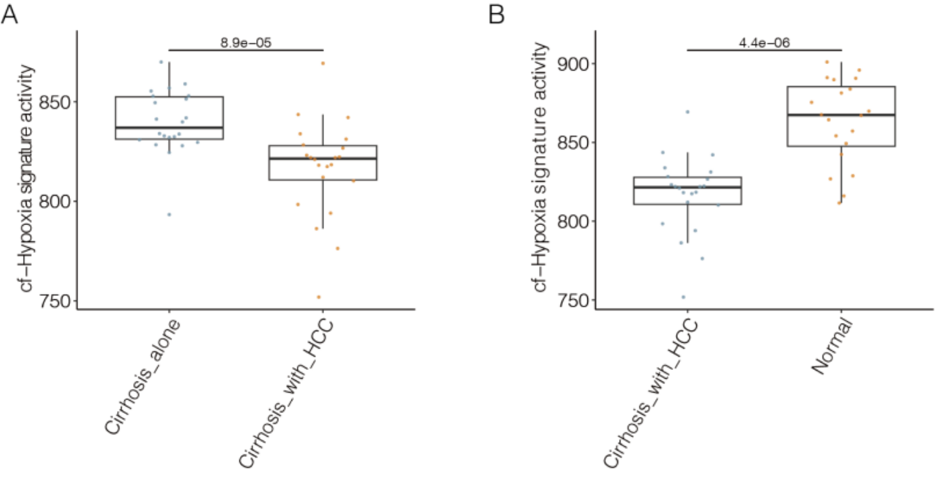
图9 缺氧有关的游离肿瘤DNA甲基化标签的活性变化
A.肝癌和肝炎血液里的缺氧有关的DNA甲基化标签活性的差异;B. 肝癌和正常人血液里的缺氧有关的DNA甲基化标签活性的差异。
肝癌血液游离的DNA甲基化标签
3.肝癌血液游离DNA甲基化标签的提取
对22例带有肝炎的肝癌血液和22例正常人血液的DNA甲基化芯片数据进行质控,过滤低质量探针位点,获得470,043个探针。对这些探针在肝癌和正常人血液的甲基化值进行置换检验,每个探针置换1000次。选择置换检验结果的P-value ≤ 0.001的探针位点,获得267,756个探针。为了获得更加稳定保守的肿瘤特异的DNA甲基化位点,选择每个探针的()的中位数作为该探针的在血液水平的甲基化值(),分别选择> 0上限和< 0下限的0.25%的值的探针,定义为高甲基化差异性位点(Hyper-DMPs, N = 2,259)和低甲基化差异性位点(Hypo-DMPs,N = 4,323)。然后,采用NMF的方法对这些保守的DMPs进行矩阵分解,根据获得评估分解结果的共识矩阵热图(图10),最终定义2个高甲基化标签(cf.Hyper.MS1,cf.Hyper.MS2)和2个低甲基化标签(cf.Hypo.MS1,cf.Hypo.MS2)。
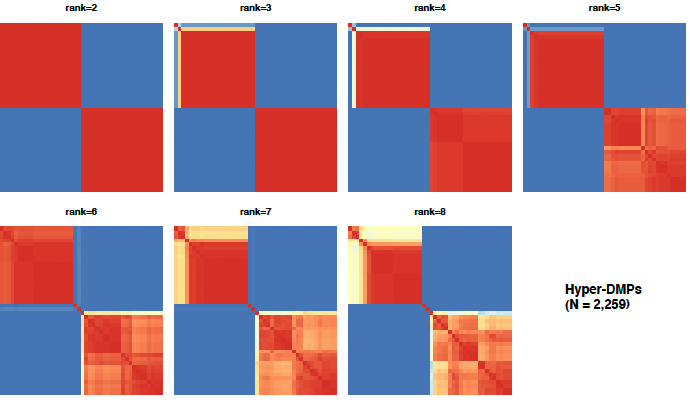
图10. NMF对高甲基化位点和低甲基化位点进行矩阵分解
4. 肝癌血液游离DNA甲基化标签的活性分布
申请人在血液游离DNA甲基化标签的活性分布图发现,血液水平的DNA甲基化标签在肿瘤样本和正常人样本出现明显的差别(图11)。
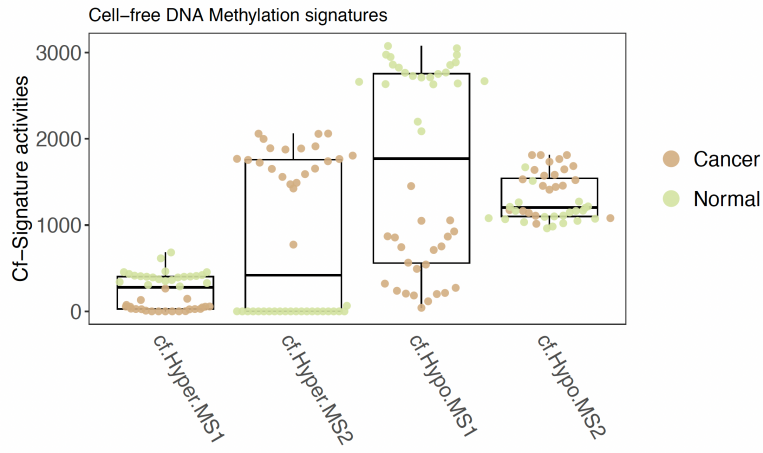
图11. 血液游离DNA甲基化标签活性分布
5. 血液游离DNA甲基化标签活性对肿瘤诊断的预测效力
鉴于血液游离DNA甲基化标签的活性在肿瘤患者和正常人之间的分布出现差异,申请人继续探查标签的活性能否预测肿瘤的发生。ROC曲线结果显示,DNA甲基化标签对肿瘤的预测效果很好,最高AUC值为1(图12)。
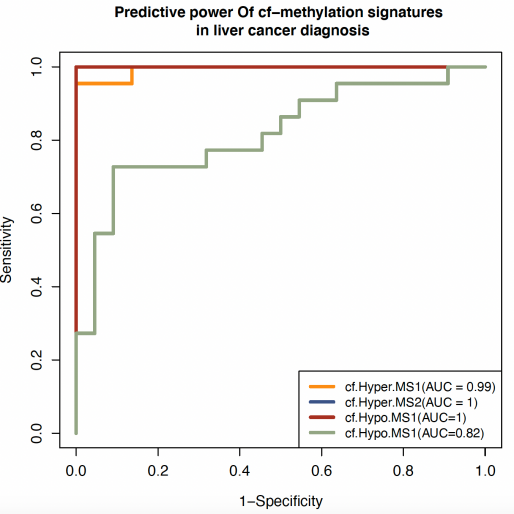
图12. 血液游离DNA甲基化标签的ROC曲线图
成果总结:
申请人主要致力于肿瘤的表观遗传学发生的机制研究,将前期发现的研究成果应用于肿瘤临床的诊断和治疗。申请人在初期的转化研究发现,肿瘤DNA甲基化的标签在临床的诊断效力相比于传统的诊断标志物具有极高的稳定性和准确性,在肿瘤的早期诊断应用上有极大的应用前景。因此,申请人将采用此研究成果推广到临床上,为肿瘤的诊断和治疗提供新的方法。
 揭榜条件
揭榜条件
①企业规模:省内登记注册一年以上的法人实体单位(企事业科研单位或相关领域内企业),能够按照承诺书要求,提供成果转化的资金、设备等配套条件。
②发展领域:医药、生物制药相关领域。
③生产方式:通过样本采集、样本处理、DNA提取、基因测序、数据分析、生成结果的方式进行生产。









 关注清华海峡研究院
关注清华海峡研究院